Terapia światłem czerwonym (ang. Red Light Therapy, RLT), znana również jako terapia laserem niskoenergetycznym (LLLT) lub fotobiomodulacja (PBM), to nieinwazyjna metoda wykorzystująca światło o określonej długości fali (najczęściej 620–750 nm dla światła czerwonego i 750–1100 nm dla bliskiej podczerwieni). Coraz więcej badań naukowych potwierdza jej skuteczność w leczeniu schorzeń oraz regeneracji skóry, redukcji bólu, regeneracji mięśni oraz poprawie funkcji neurologicznych. Efekty kliniczne terapii światłem czerwonym mają solidne podstawy w mechanizmach molekularnych i komórkowych.
Mechanizmy molekularne i komórkowe
Światło czerwone i bliska podczerwień przenikają przez tkanki i są absorbowane głównie przez chromofory* w mitochondriach, a szczególnie przez oksydazę cytochromu c (CCO) – kluczowy enzym łańcucha oddechowego. Po absorpcji światła w odpowiednim zakresie, dochodzi do szeregu korzystnych procesów biologicznych:
- Zwiększona produkcja ATP
Pobudzenie aktywności CCO skutkuje zwiększeniem potencjału błony mitochondrialnej, co prowadzi do wzrostu produkcji adenozynotrójfosforanu (ATP) – podstawowego nośnika energii w komórkach. Większa ilość energii wspomaga procesy naprawcze i regeneracyjne [1]. - Modulacja reaktywnych form tlenu (ROS)
Nadmiar produkcji reaktywnych form tlenu prowadzi do starzenia komórkowego. Jednakże krótkotrwały wzrost reaktywnych form tlenu jest korzystny, gdyż działa jak sygnał, który aktywuje mechanizmy obronne komórki, w tym szlaki antyoksydacyjne zależne od czynnika transkrypcyjnego** Nrf2, zwiększając odporność komórki na stres oksydacyjny [2]. - Ekspresja genów i sygnalizacja komórkowa
Ekspozycja na światło aktywuje także inne czynniki transkrypcyjne, takie jak NF-κB i AP-1, które regulują geny związane z zapaleniem, proliferacją i naprawą komórek [3]. - Uwolnienie tlenku azotu (NO)
Terapia światłem czerwonym powoduje uwolnienie tlenku azotu z kompleksów mitochondrialnych, co poprawia funkcjonowanie mitochondriów (NO hamuje aktywność oksydazy cytochromu c) i prowadzi do rozszerzenia naczyń krwionośnych, poprawiając ukrwienie tkanek [4]. - Aktywacja komórek macierzystych
RLT może aktywować mezenchymalne komórki macierzyste oraz wspierać ich migrację i różnicowanie, co sprzyja procesom regeneracyjnym [5]. Macierzyste komórki mezenchymalne, występują głównie, choć nie tylko, w szpiku kostnym i mogą różnicować w komórki kości, chrząstki, a także w komórki tłuszczowe.
*Chromofory w mitochondriach to cząsteczki, które pochłaniają światło (czyli energię elektromagnetyczną) o określonych długościach fali i przekształcają ją w energię biologicznie aktywną. W kontekście terapii światłem czerwonym najważniejszym chromoforem jest:
Oksydaza cytochromu c (CCO). Jest to enzym znajdujący się w łańcuchu oddechowym mitochondriów, odpowiadający za końcowy etap produkcji ATP – energii wykorzystywanej przez komórki. CCO pochłania światło z zakresu czerwonego (620–660 nm) i bliskiej podczerwieni (810–850 nm).
**Czynniki transkrypcyjne są to białka, które modulują transkrypcję, czyli aktywność (ekspresję) genów.

Kliniczne korzyści terapii światłem czerwonym
Zdrowie skóry
RLT pobudza syntezę kolagenu, poprawia jędrność skóry, redukuje zmarszczki i przyspiesza gojenie ran. Komórki takie jak fibroblasty, keratynocyty i komórki śródbłonka reagują pozytywnie na terapię światłem czerwonym. Udowodniono znaczną poprawę struktury skóry po kilku tygodniach stosowania terapii [6].
Redukcja bólu i stanów zapalnych
Terapia ta zmniejsza produkcję cytokin prozapalnych (np. IL-6, TNF-α), jednocześnie zwiększając poziom cytokin przeciwzapalnych (np. IL-10). Metaanaliza wykazała znaczną redukcję bólu u pacjentów z chorobami układu mięśniowo-szkieletowego [7].
Regeneracja mięśni i wydolność fizyczna
RLT wspomaga regenerację mięśni po wysiłku, zmniejsza ból mięśniowy i stres oksydacyjny. Wykazano, że terapia poprawia regenerację i siłę mięśni poprzez zwiększenie aktywności mitochondrialnej [8].
Funkcje neurologiczne
Światło bliskiej podczerwieni przenika przez czaszkę i poprawia funkcjonowanie mitochondriów w neuronach, wspierając neurogenezę, synaptogenezę i redukując neurozapalne procesy. Zaobserwowano poprawę funkcji poznawczych u pacjentów z urazowym uszkodzeniem mózgu (TBI) po zastosowaniu terapii LED [9].
Typowe protokoły terapii światłem czerwonym
Choć protokoły różnią się w zależności od celu terapii, zastosowanej technologii i indywidualnych potrzeb pacjenta, poniżej przedstawiono ogólne wytyczne oparte na aktualnych badaniach klinicznych i praktykach terapeutycznych:
Czas trwania jednej sesji
- Typowy zakres: od 5 do 20 minut.
- W przypadku głębszych tkanek (np. stawy, mięśnie) sesje mogą być dłuższe (do 30 minut), zwłaszcza przy stosowaniu światła bliskiej podczerwieni.
Częstotliwość terapii
- Zalecana częstość: 2–5 razy w tygodniu.
- W terapii ostrej (np. gojenie ran, ból mięśni) stosuje się nawet codzienne sesje przez pierwsze 1–2 tygodnie.
- W przypadkach przewlekłych (np. artretyzm, TBI) sesje wykonuje się 2–3 razy tygodniowo przez kilka tygodni lub miesięcy.
Długość fal
- Czerwone światło (620–660 nm) – skuteczne w terapiach powierzchniowych: skóry, gojenia ran, przeciwstarzeniowych.
- Bliska podczerwień (810–850 nm) – penetruje głębiej i jest stosowana w leczeniu mięśni, stawów, mózgu i nerwów.
Dawka światła (energia)
- Wyrażana jako dawka energii w J/cm² (dżule na centymetr kwadratowy).
- Typowy zakres terapeutyczny: 4–10 J/cm² dla zastosowań powierzchniowych, 10–50 J/cm² dla tkanek głębokich.
Moc światła (irradiancja)
- Optymalna moc wyjściowa: 20–200 mW/cm².
- Wyższe wartości pozwalają na krótsze sesje przy tej samej dawce energii.
Odległość od źródła światła
- Zwykle: 5–30 cm od skóry.
- Im większa moc urządzenia, tym większy może być dystans bez utraty efektywności.
Rodzaje urządzeń
- LED-y i lasery to najczęstsze źródła światła.
- Lasery mają węższe spektrum i większą moc punktową, ale LED-y są tańsze i odpowiednie do użytku domowego.
Przykładowe zastosowania i protokoły
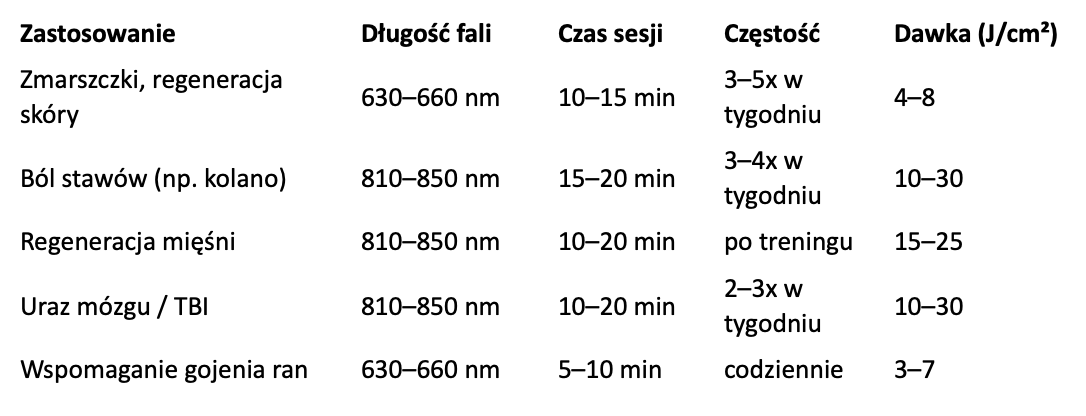
Terapia Światłem Czerwonym (RLT) – Podsumowanie
Terapia światłem czerwonym (Red Light Therapy – RLT) to nieinwazyjna metoda wspomagająca regenerację tkanek, łagodzenie bólu, poprawę wyglądu skóry i zdrowia ogólnego. Wykorzystuje światło o długości fali z zakresu czerwieni i bliskiej podczerwieni (620–850 nm), które przenika do komórek i pobudza ich aktywność.
Światło czerwone działa na mitochondria – „elektrownie komórkowe” – zwiększając produkcję energii (ATP). Efekty biologiczne:
- więcej energii w komórkach,
- redukcja stanów zapalnych,
- lepsze krążenie krwi,
- aktywacja naturalnych mechanizmów naprawczych.
Korzyści terapeutyczne wynikające ze stosowania RLT
- Poprawa kondycji skóry (zmniejszenie zmarszczek, trądziku, przebarwień)
- Redukcja bólu mięśni i stawów
- Przyspieszenie regeneracji po treningu
- Wspomaganie pracy mózgu i koncentracji
- Przyspieszenie gojenia ran i urazów
---
Bibliografia
- Hamblin, M. R. (2017). Mechanisms and applications of the anti-inflammatory effects of photobiomodulation. AIMS Biophysics, 4(3), 337–361.
- Pires, D. et al. (2011). Low-level laser therapy (LLLT) and its anti-inflammatory effects: a literature review. Lasers in Medical Science, 26(3), 589–597.
- Karu, T. I. (1999). Primary and secondary mechanisms of action of visible to near-IR radiation on cells. J Photochem Photobiol B, 49(1), 1–17.
- Lane, N. (2006). Cell biology: power games. Nature, 443(7114), 901–903.
- Mvula, B. et al. (2010). Effect of low-level laser irradiation and epidermal growth factor on adult human adipose-derived stem cells. Lasers in Medical Science, 25(1), 33–39.
- Avci, P. et al. (2013). Low-level laser (light) therapy (LLLT) in skin: stimulating, healing, restoring. Seminars in Cutaneous Medicine and Surgery, 32(1), 41–52.
- Stausholm, M. B. et al. (2019). Efficacy of low‐level laser therapy on pain and disability in knee osteoarthritis. Arthritis Research & Therapy, 21(1), 1–13.
- Leal Junior, E. C. P. et al. (2009). Effect of 830 nm low‐level laser therapy in exercise‐induced skeletal muscle fatigue in humans. Photomedicine and Laser Surgery, 27(4), 645–651.
- Naeser, M. A. et al. (2014). Improved cognitive function after transcranial LED treatments in chronic traumatic brain injury. Photomedicine and Laser Surgery, 32(12), 678–686.










